Control Tower 상세 보기
17개 탭 대시보드가 FDA 여정 의 모든 측면을 관리합니다 — 가이드 설정 마법사부터 듀얼트랙 개발, FDA 커뮤니케이션 자동화, 팀 협업까지.
▶ 510(k) 라이프사이클 워크스루
Control Tower가 의료기기를 Pre-Sub에서 FDA 승인까지 어떻게 안내하는지 단계별로 확인하세요.
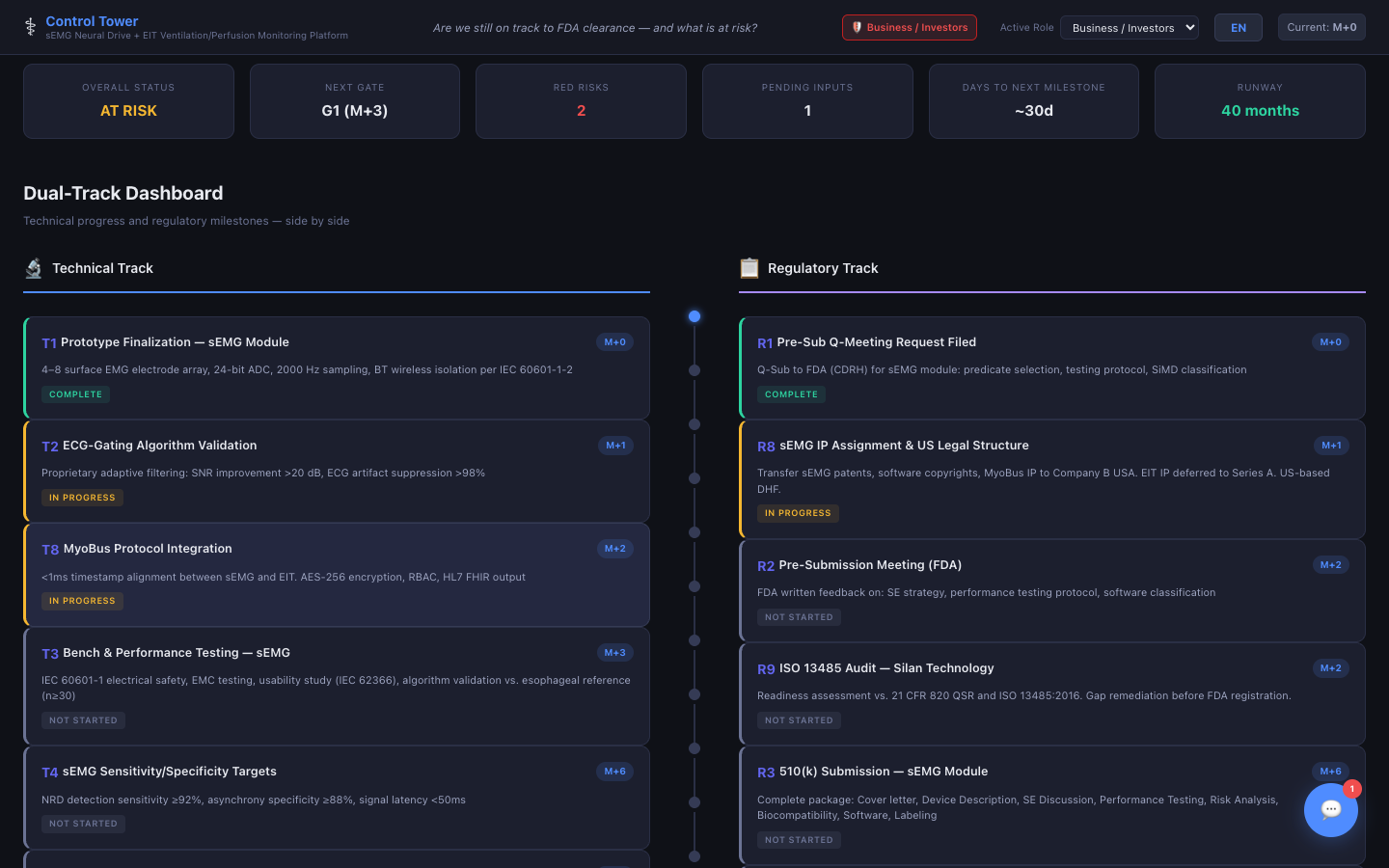
듀얼트랙 대시보드
기술과 규제 마일스톤을 병렬 추적 — 두 트랙의 진행 상황을 한눈에 파악합니다.
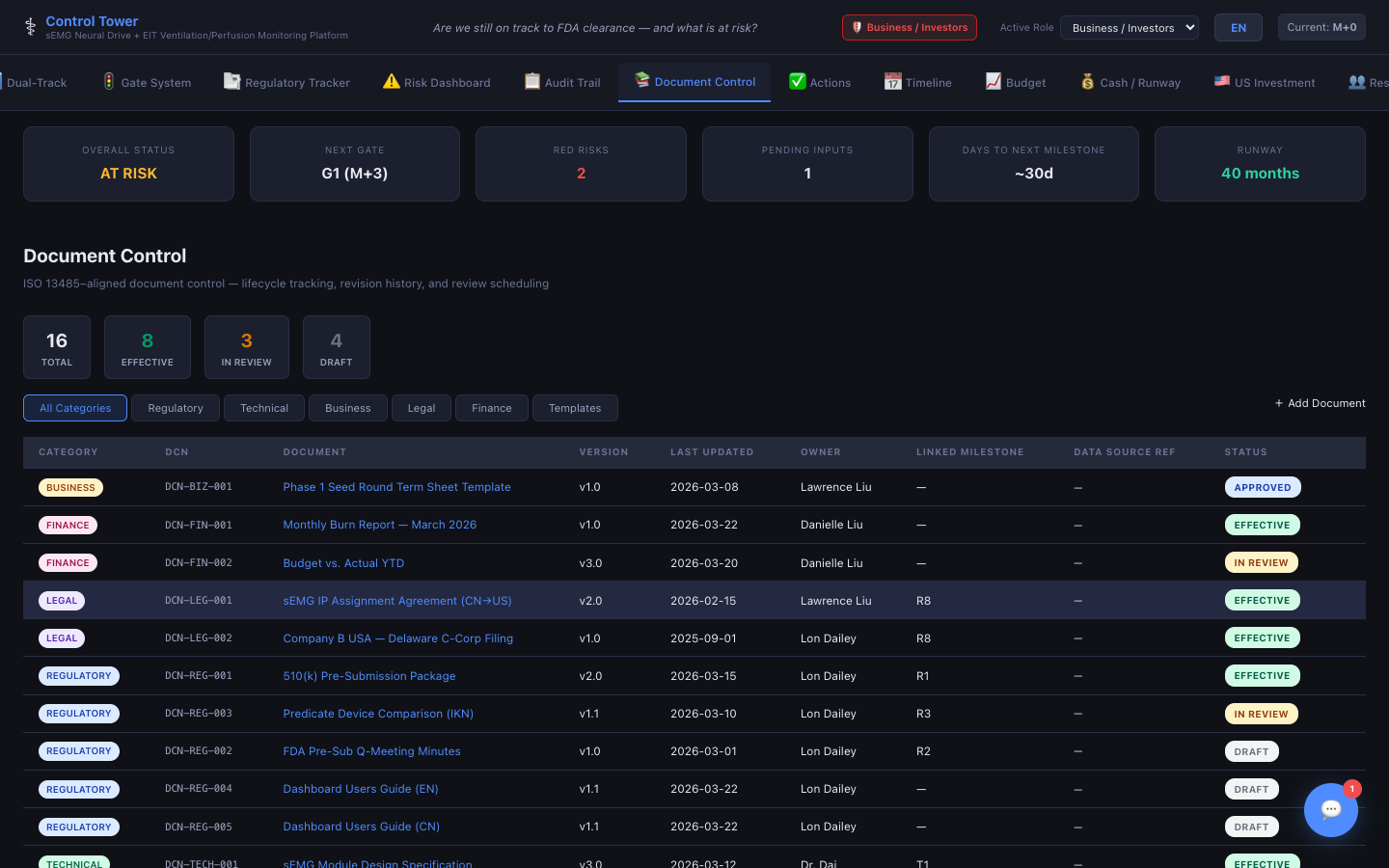
문서 관리
ISO 13485 기반 수명주기 추적 — 개정 이력, 검토 일정, 감사 추적을 포함합니다.
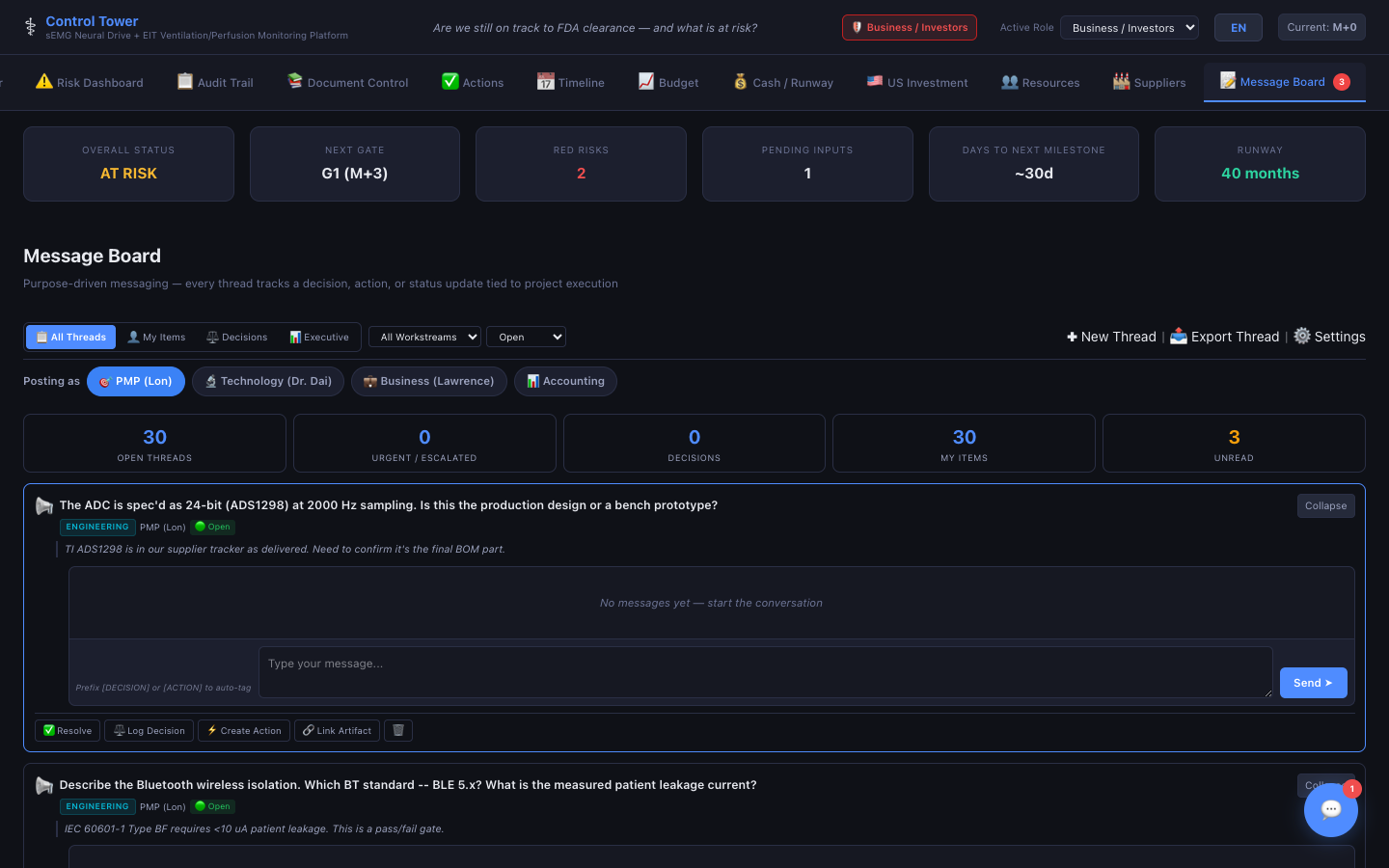
메시지 보드
목적 중심 메시징 시스템 — 모든 스레드가 프로젝트 실행에 연결된 결정, 액션, 상태 업데이트를 추적합니다.
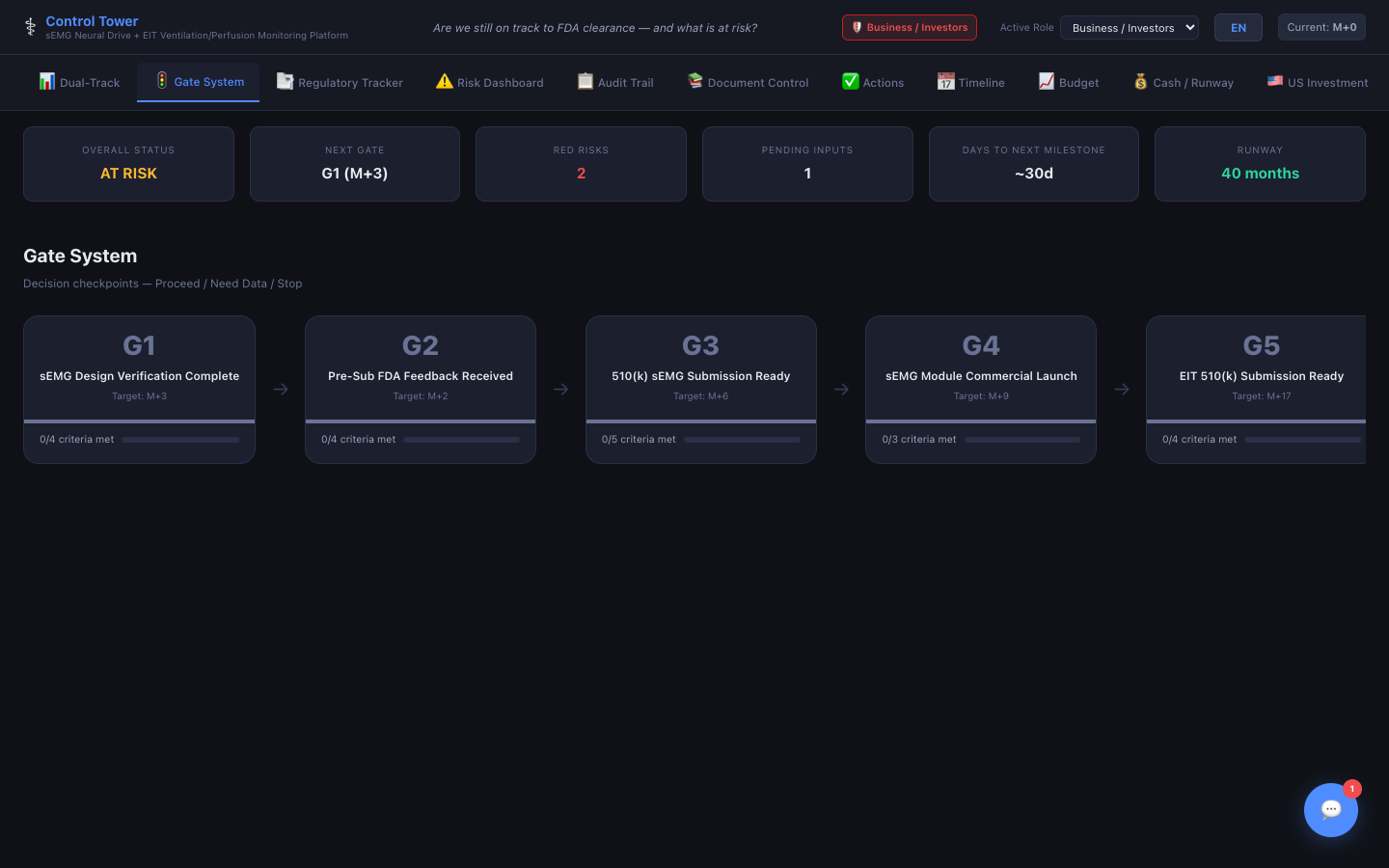
게이트 시스템
기준 체크리스트가 포함된 단계별 게이트 리뷰 — 진행/불가 결정, 이해관계자 입력 및 조건 기록.
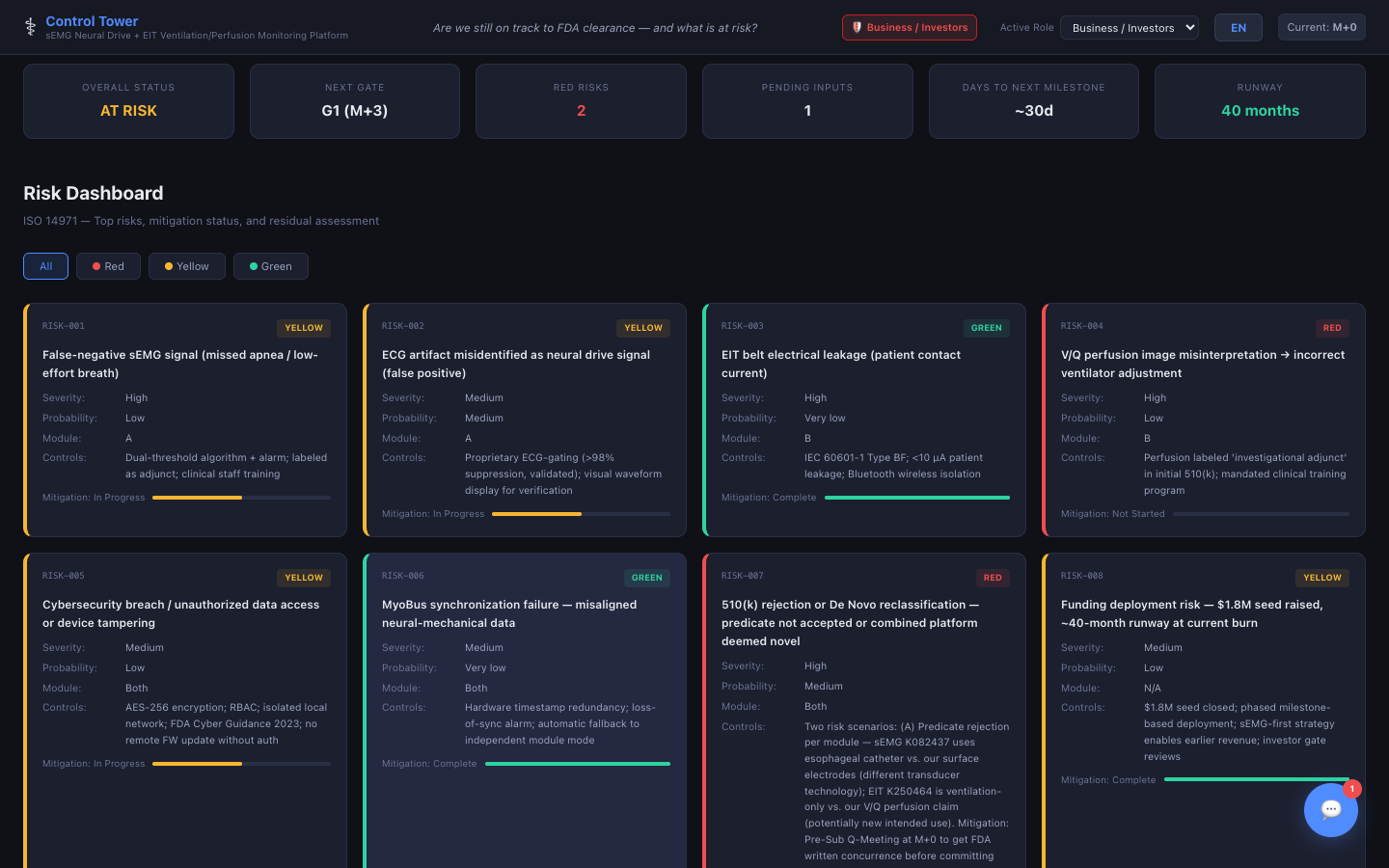
리스크 대시보드
ISO 14971 리스크 매트릭스 — 심각도, 발생확률, 색상 구분 리스크 등급으로 식별부터 종결까지 완화 조치를 추적합니다.
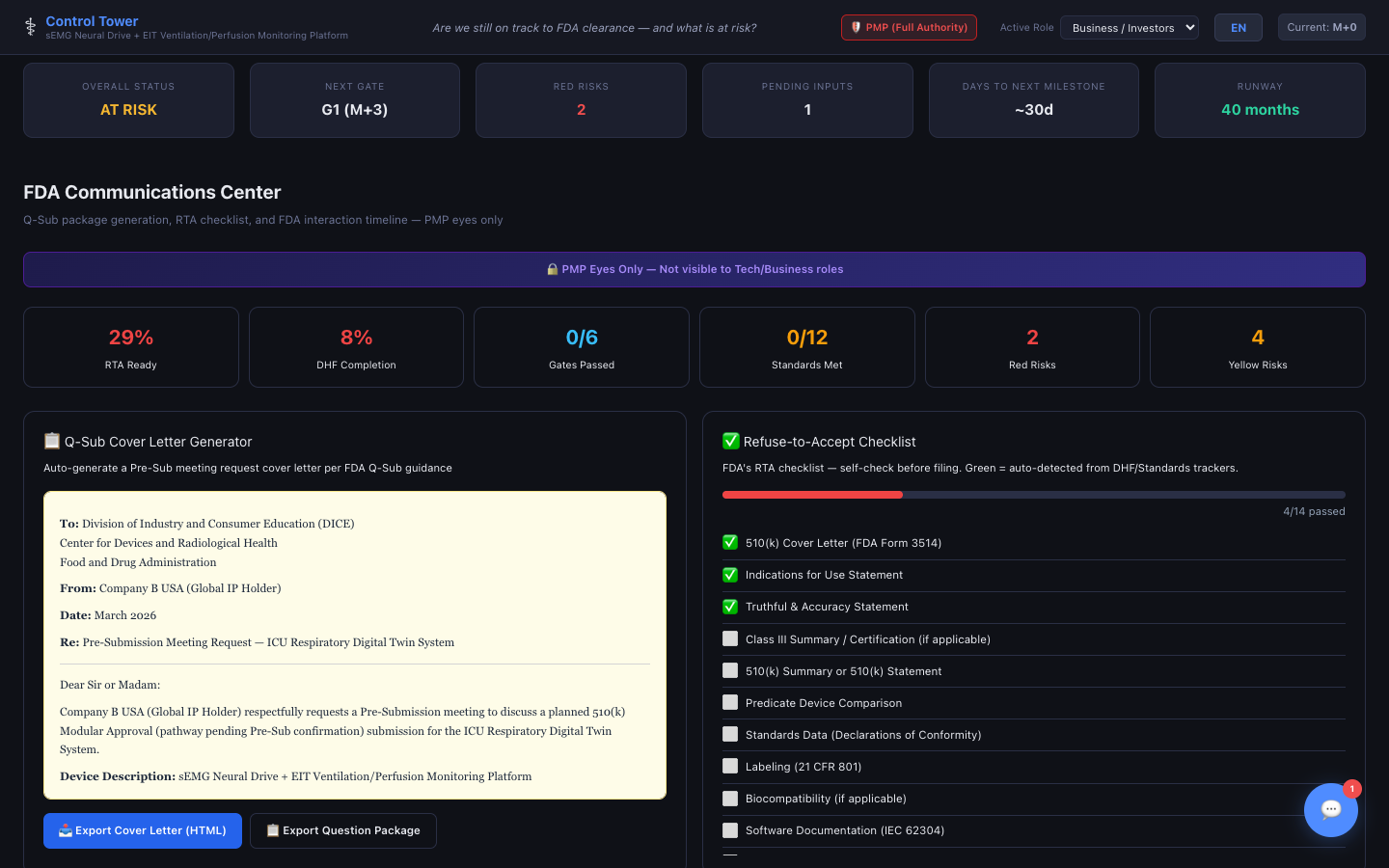
FDA 커뮤니케이션 센터
Q-Sub 커버레터 생성기, 17항 RTA 자가점검, MDUFA 90일 방사형 클록 게이지(색상 코드: 15일 차 RTA 스크리닝 → 60일 차 실질 심사 → 90일 차 결정 목표, 클록 일시정지 추적 포함), SE 의사결정 플로우차트, 타임라인 탭에 미니 일수 배지 — 하나의 플랫폼에서 모두 처리.
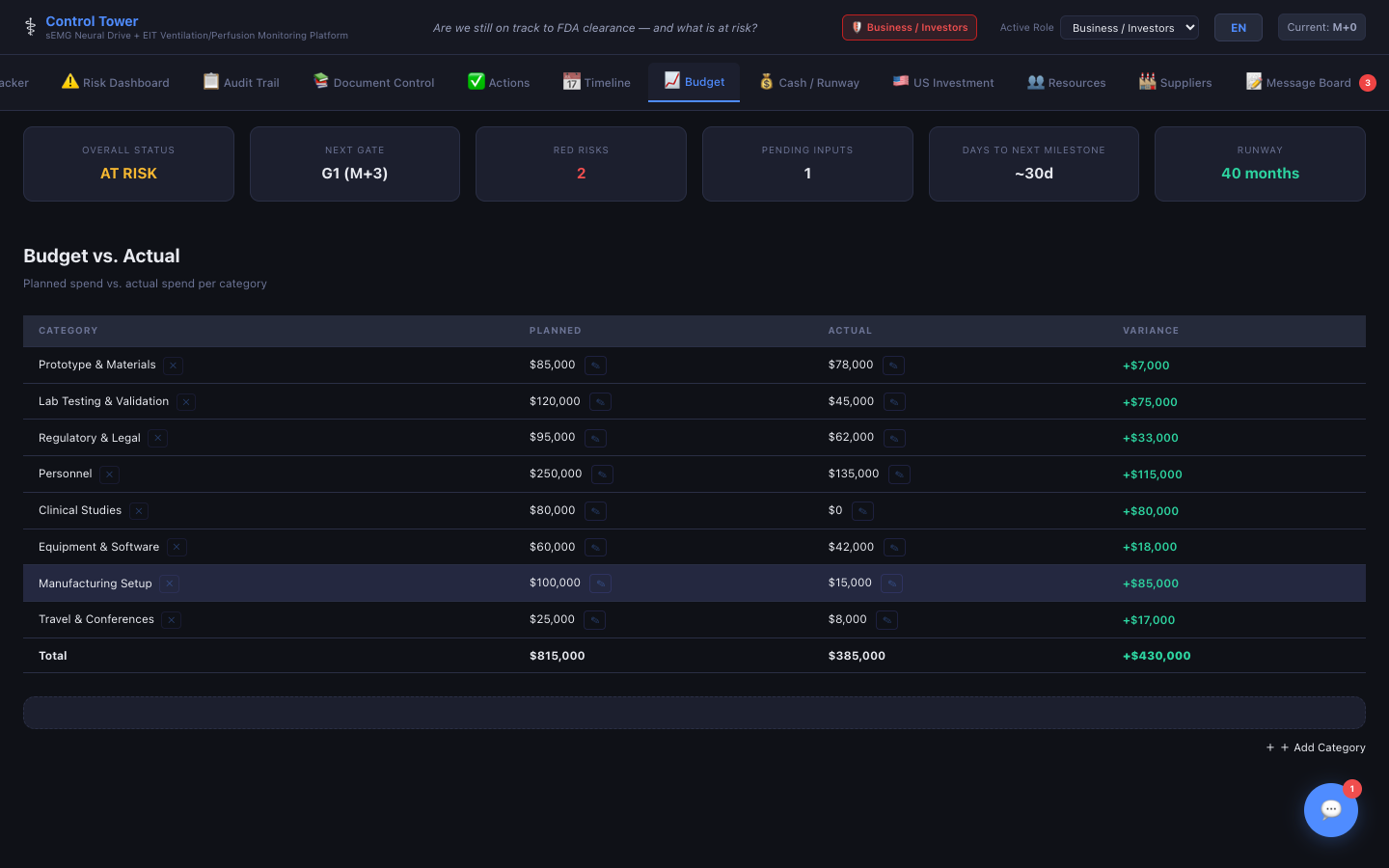
예산 추적
카테고리별 계획 대 실적 지출 및 자동 차이 계산 — USD/KRW 표시 간 전환.
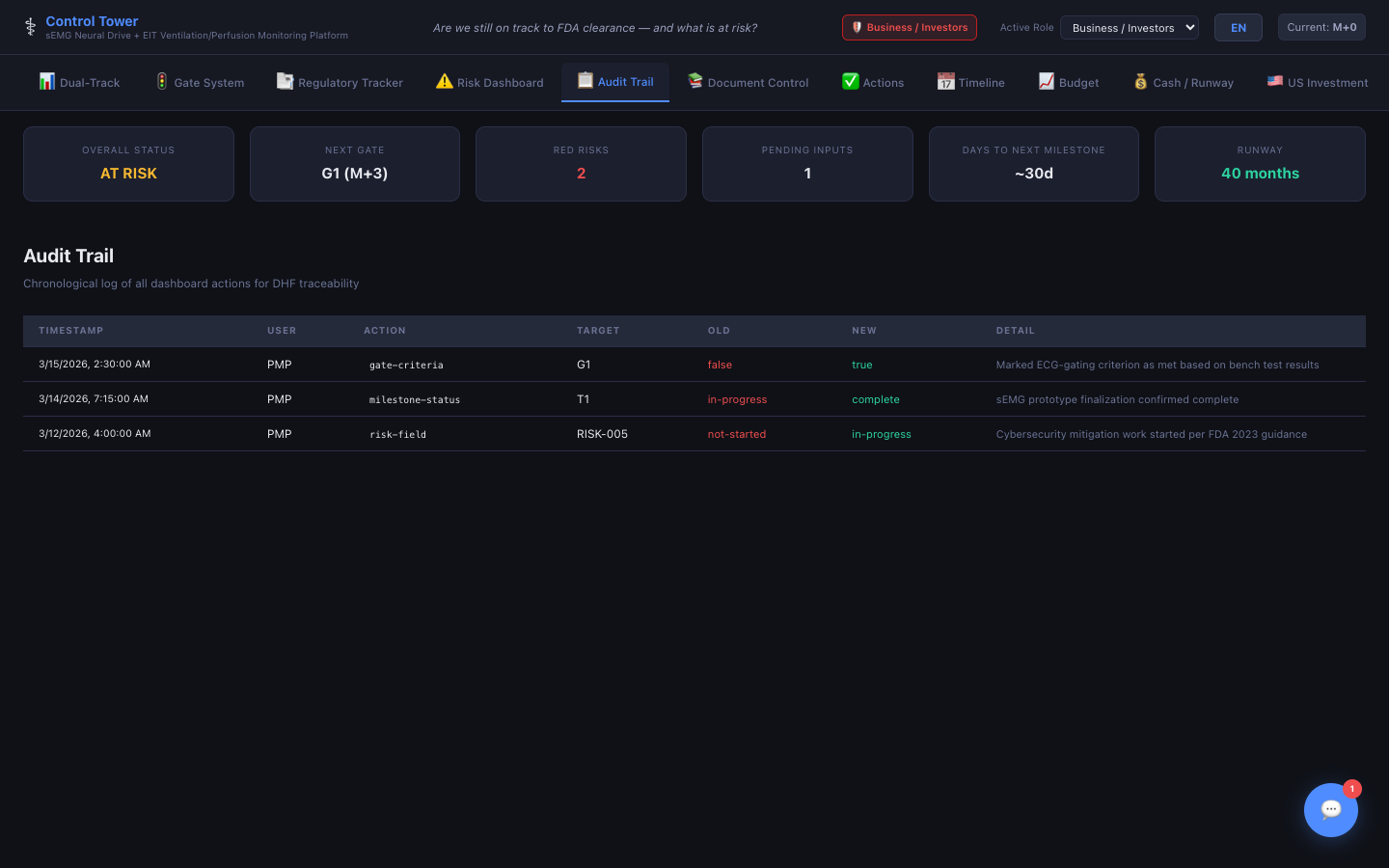
감사 추적
21 CFR Part 11 준수 — 모든 변경에 타임스탬프, 사용자, 필드, 이전 값, 새 값, 상세 설명이 기록됩니다.
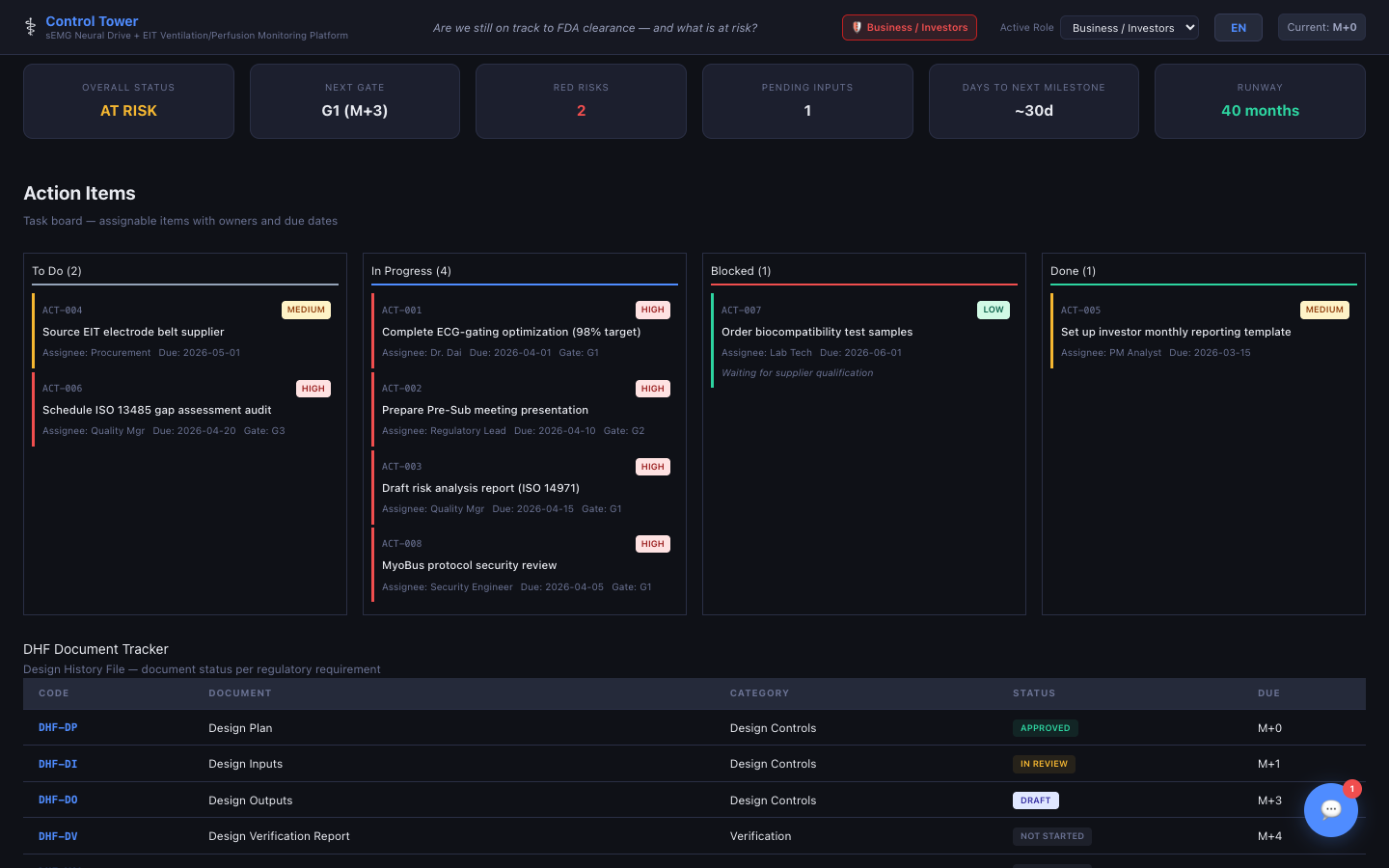
액션 항목 / DHF / CAPA
태스크 보드, 설계 이력 파일 트래커, 기기 마스터 기록 트래커, 시정 및 예방 조치 로그.
17개 탭 — 프로젝트 전체 가시화
 듀얼트랙
듀얼트랙
 게이트 시스템
게이트 시스템
 리스크 대시보드
리스크 대시보드
 감사 추적
감사 추적
 문서 관리
문서 관리
 액션 항목
액션 항목
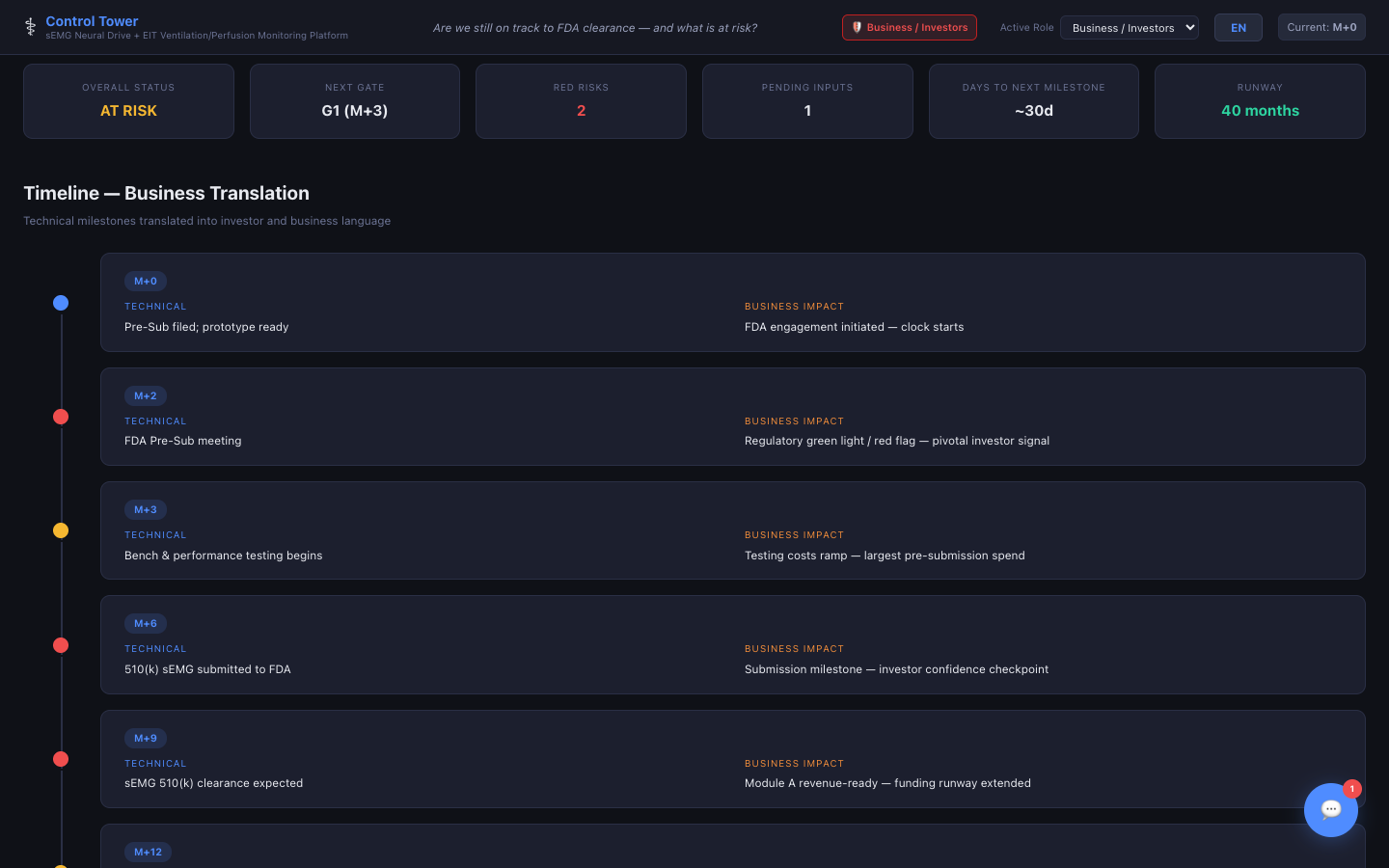 타임라인
타임라인
 예산
예산
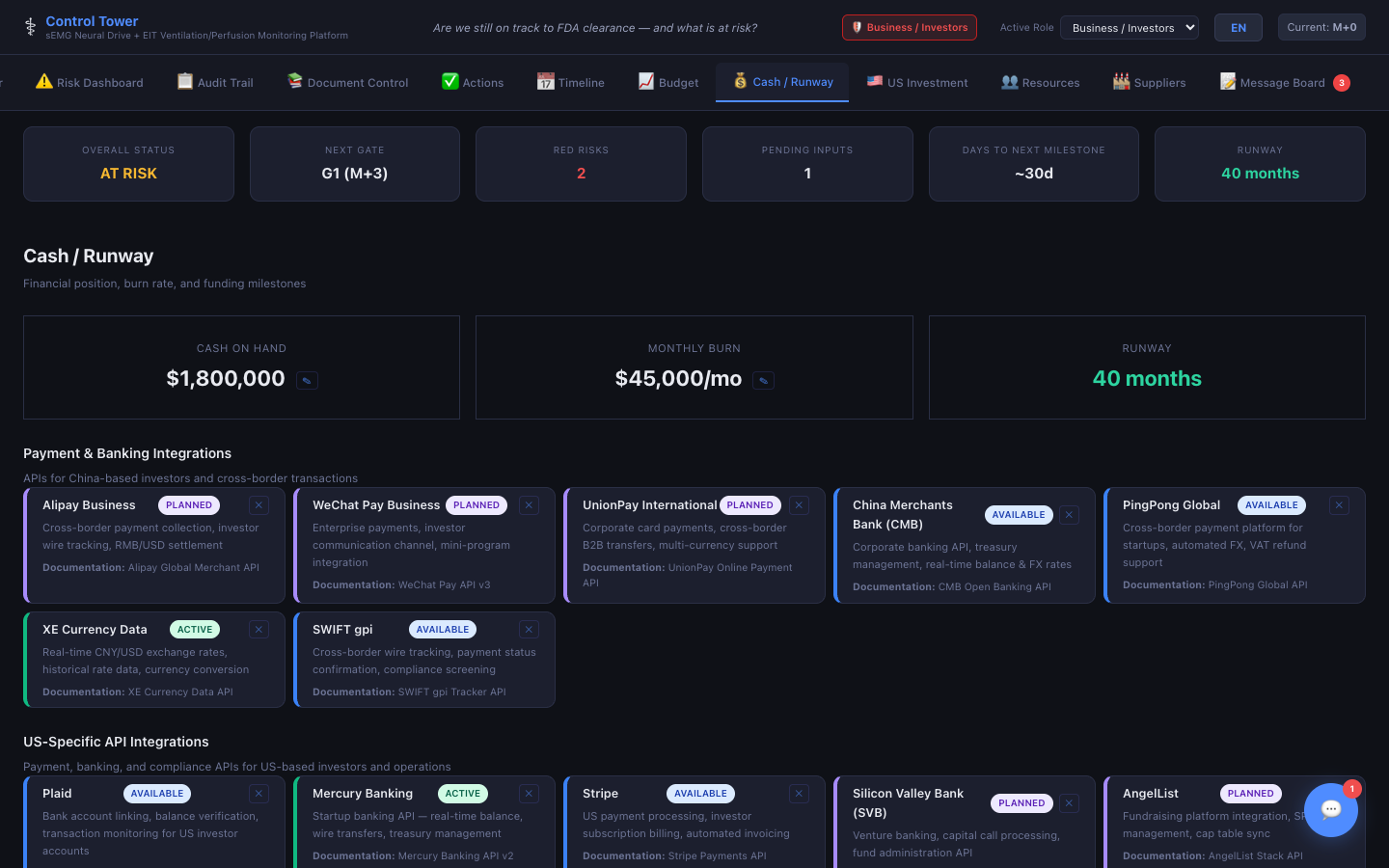 자금/런웨이
자금/런웨이
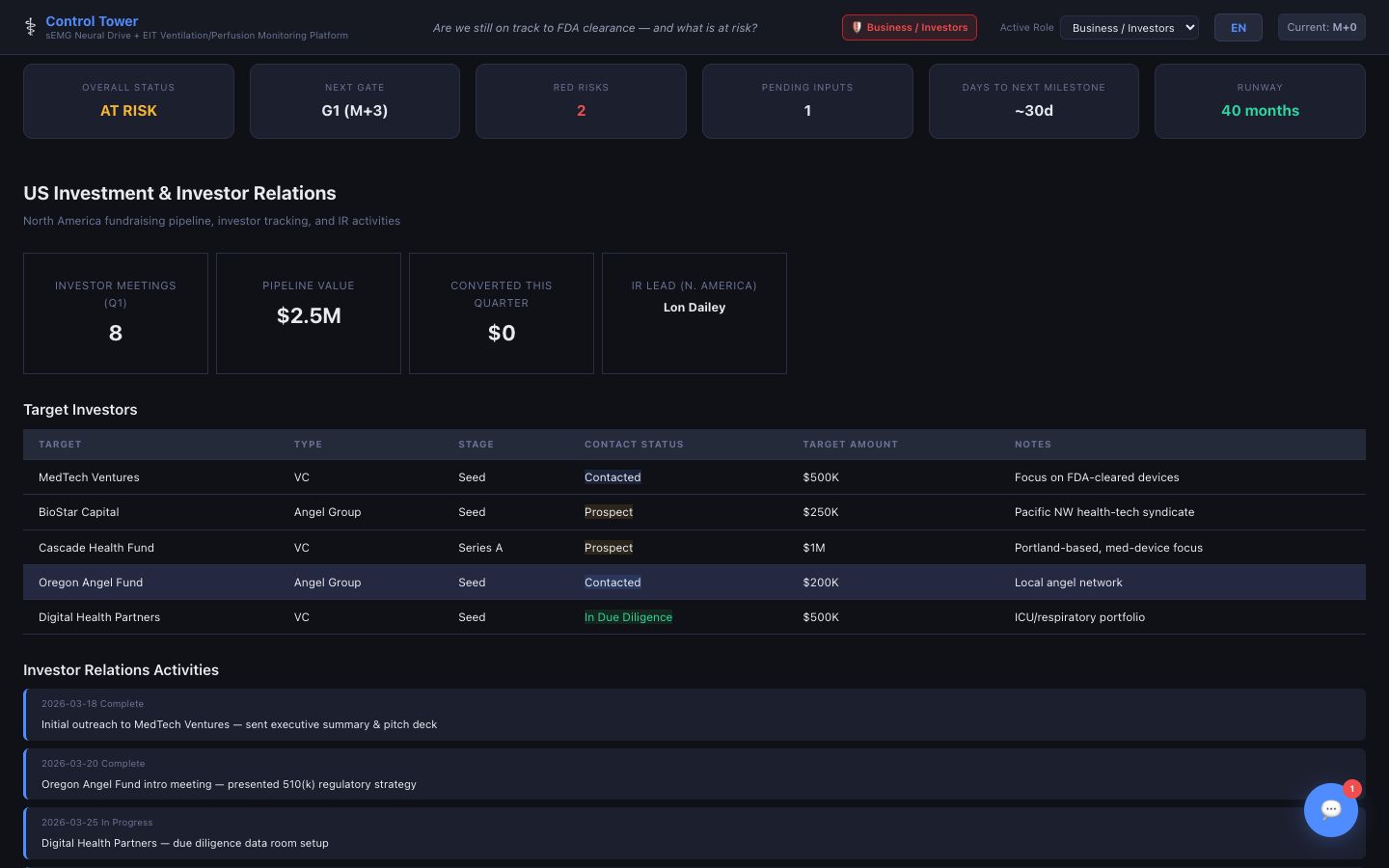 미국 투자
미국 투자
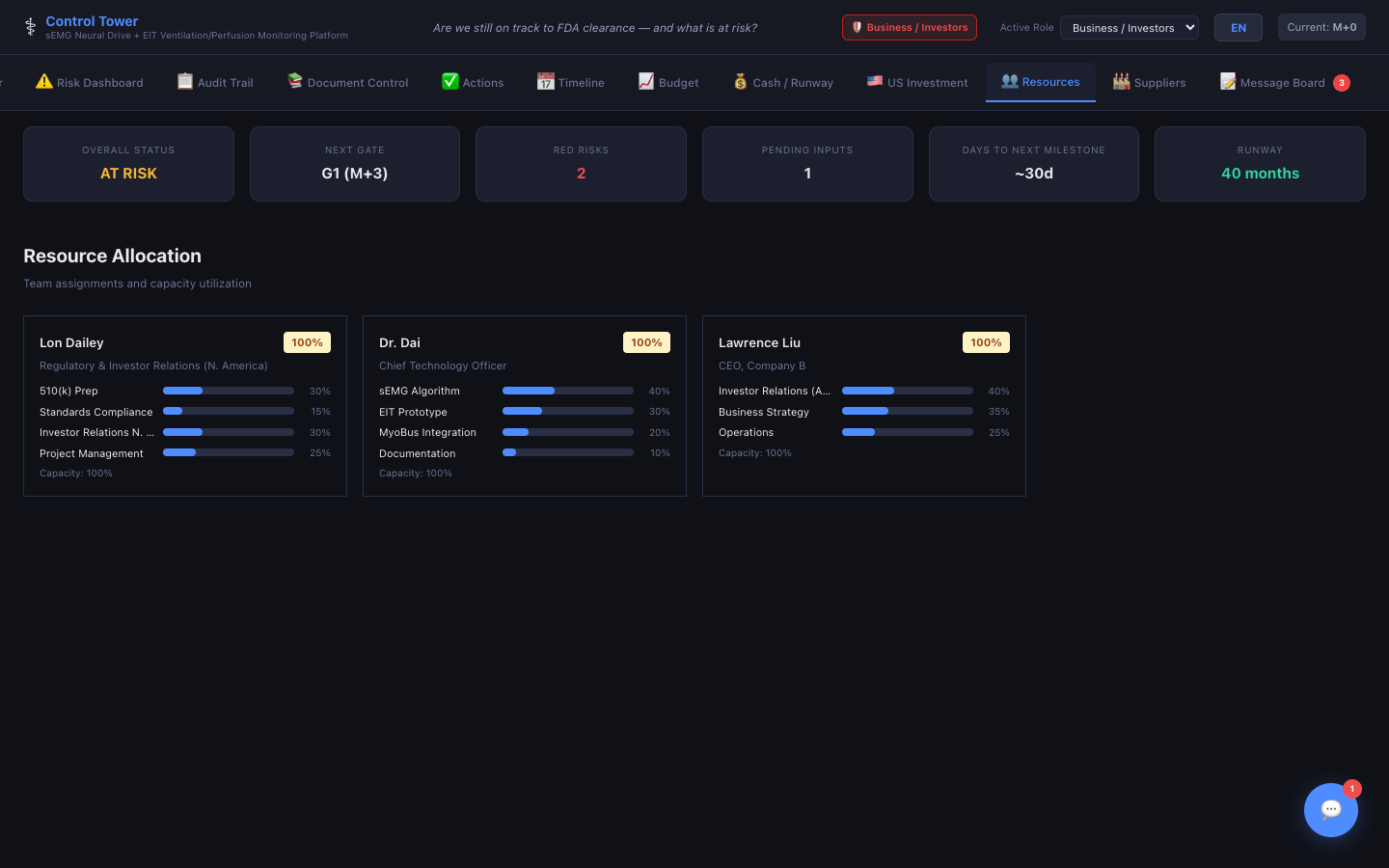 리소스
리소스
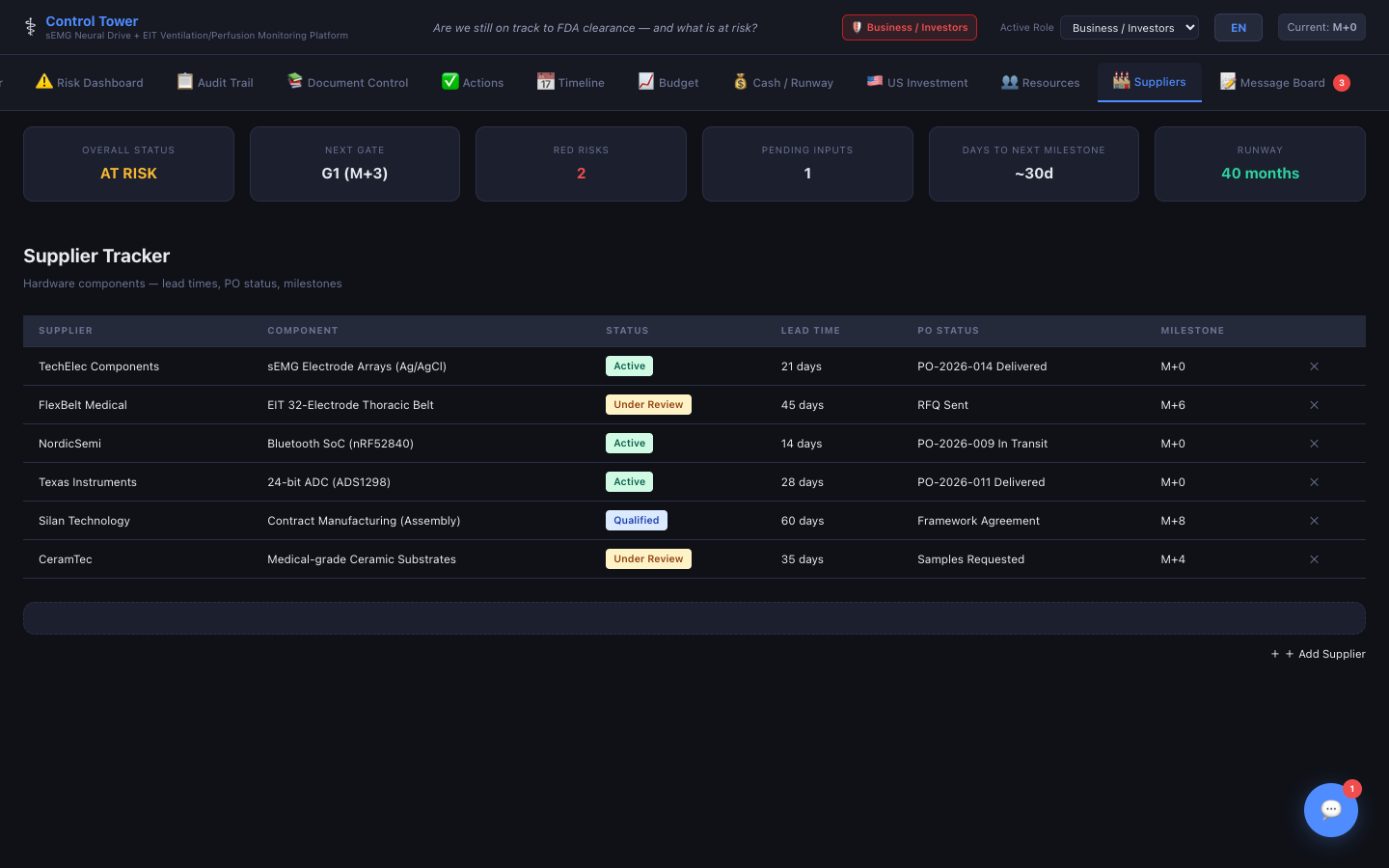 공급업체
공급업체
 메시지 보드
메시지 보드
 FDA 커뮤니케이션
FDA 커뮤니케이션
