深入了解 Control Tower
我们的17个标签仪表盘管理FDA 之旅的每一个方面——从引导式设置向导到双轨道开发、FDA通信自动化和团队协作。
▶ 510(k) 生命周期演示
了解Control Tower如何引导医疗器械从Pre-Sub到FDA审批——逐步展示。
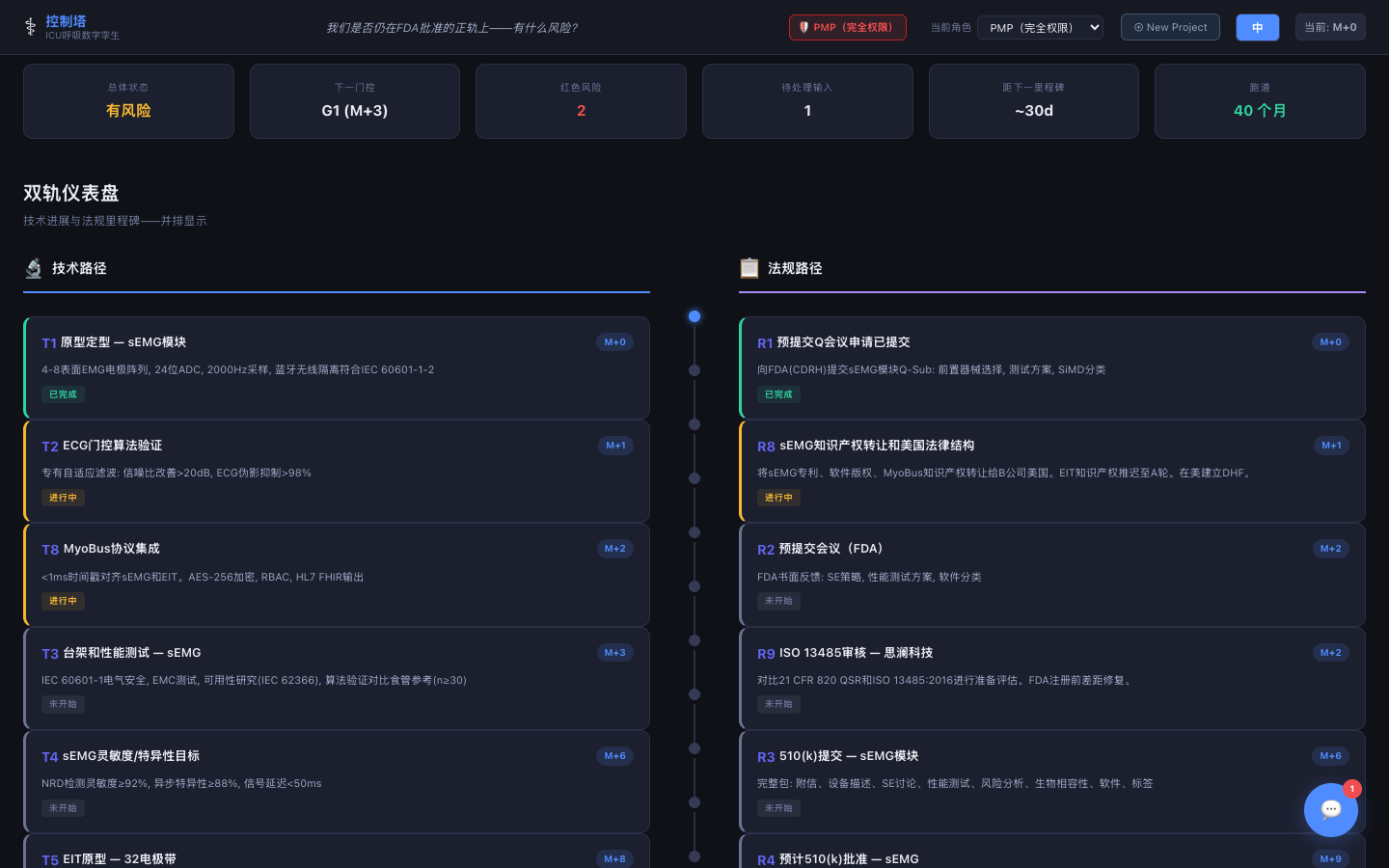
双轨道仪表盘
技术和法规里程碑并排跟踪——随时了解两条轨道的进展状态。
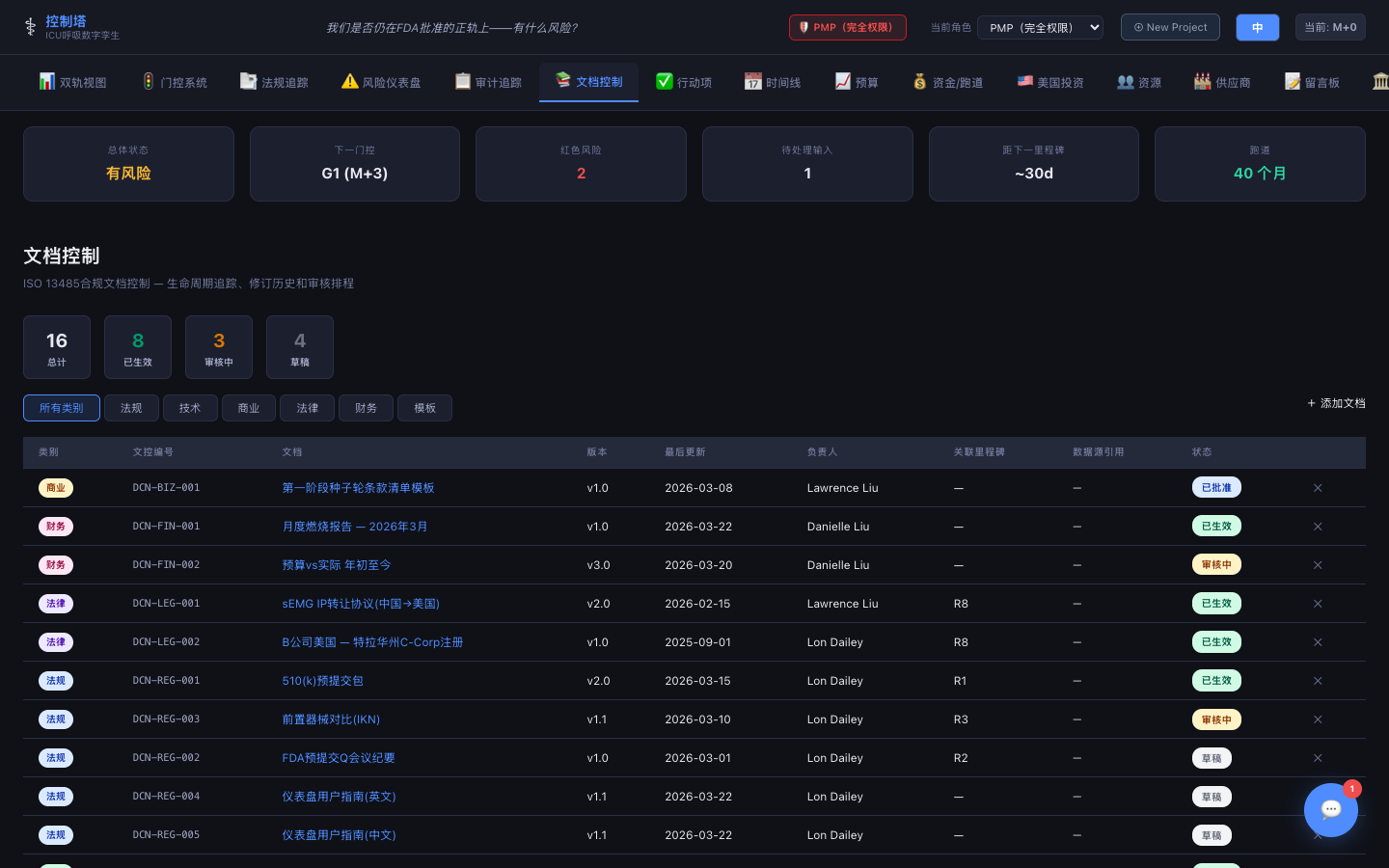
文档控制
符合ISO 13485的生命周期跟踪,包含版本历史、评审安排和审计追溯。
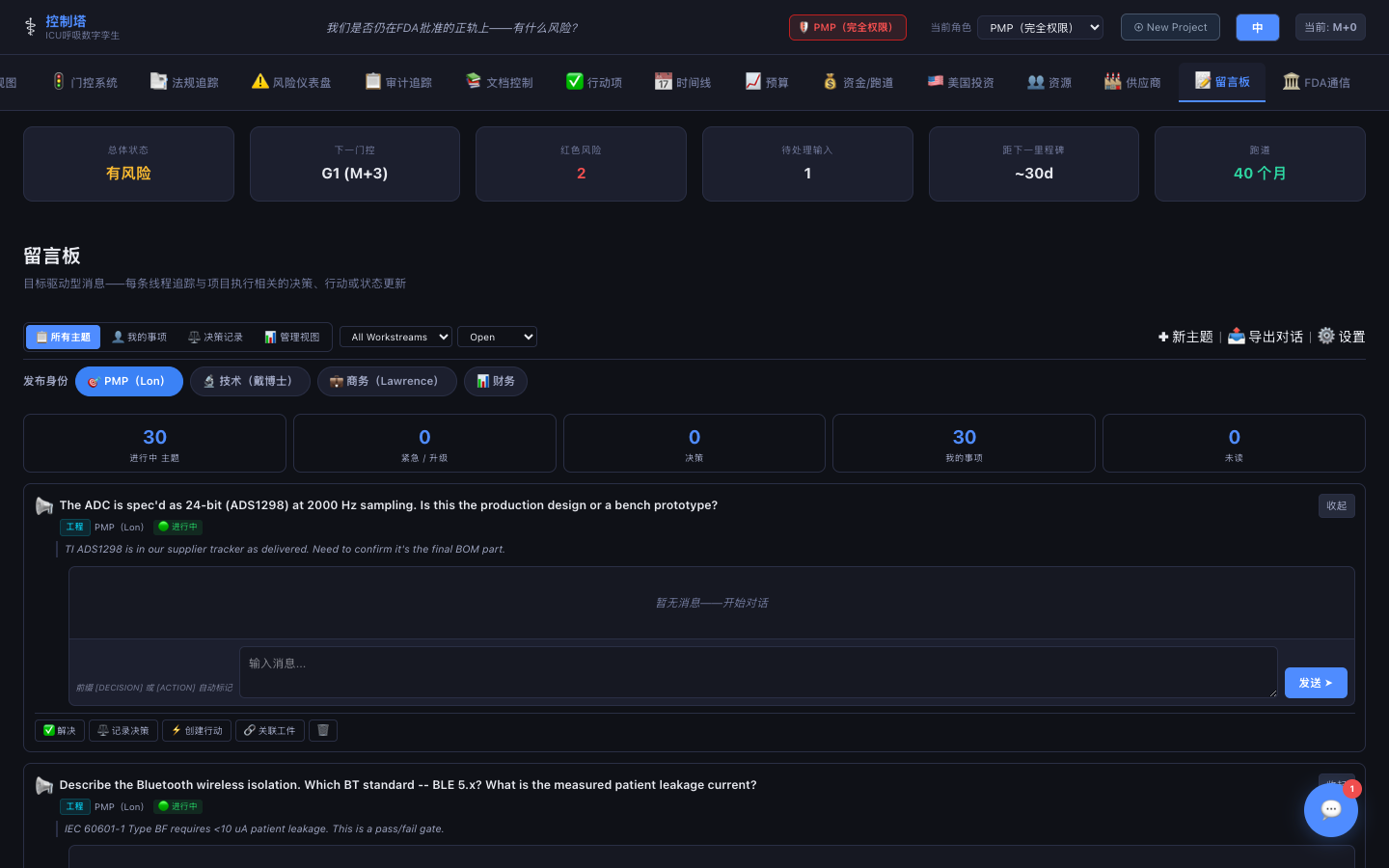
消息中心
目标驱动的消息系统——每条线程追踪一个决策、行动或状态更新,与项目执行紧密结合。
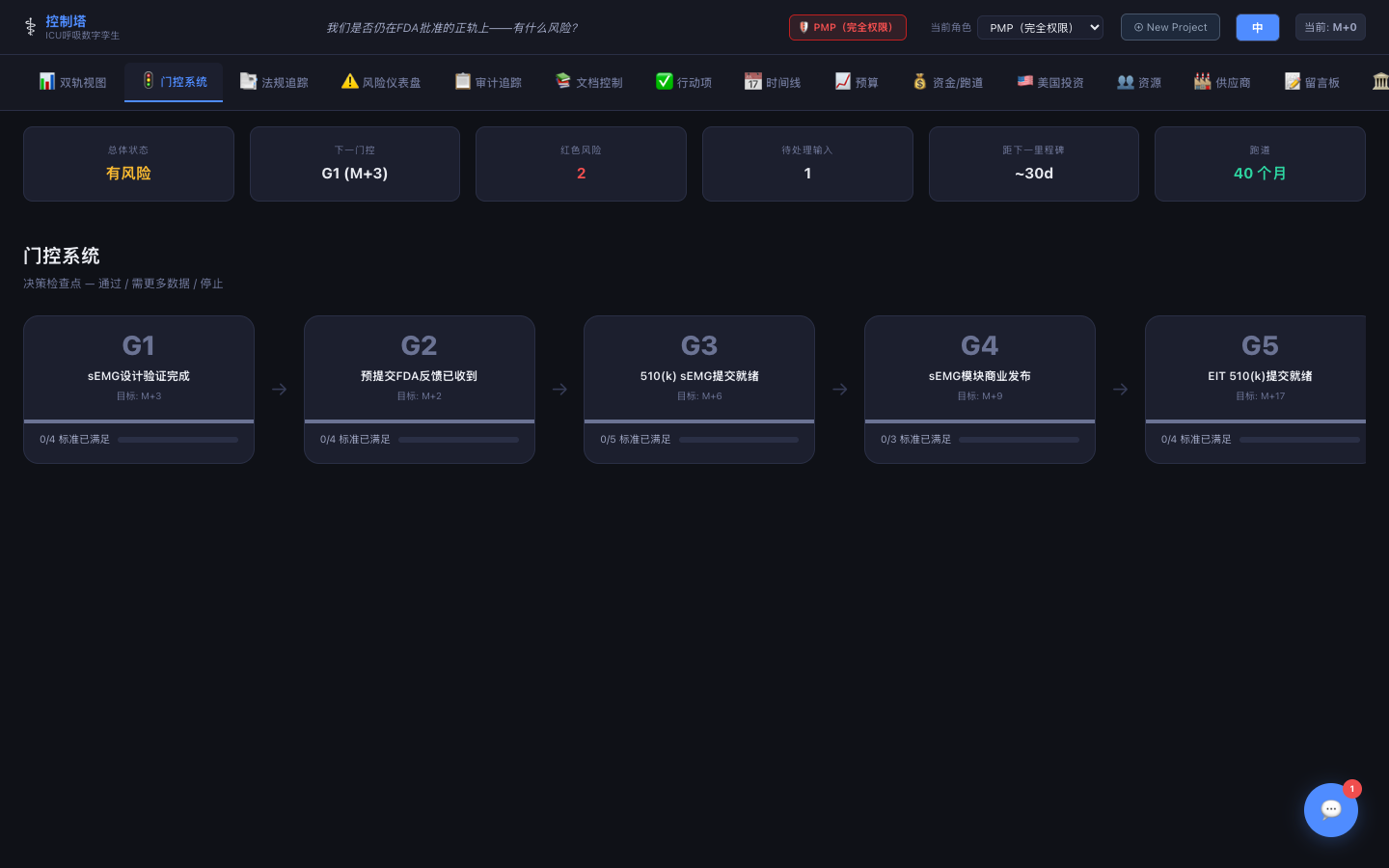
门控系统
带标准清单的阶段门控评审——通过/不通过决定,记录利益相关方输入和条件。
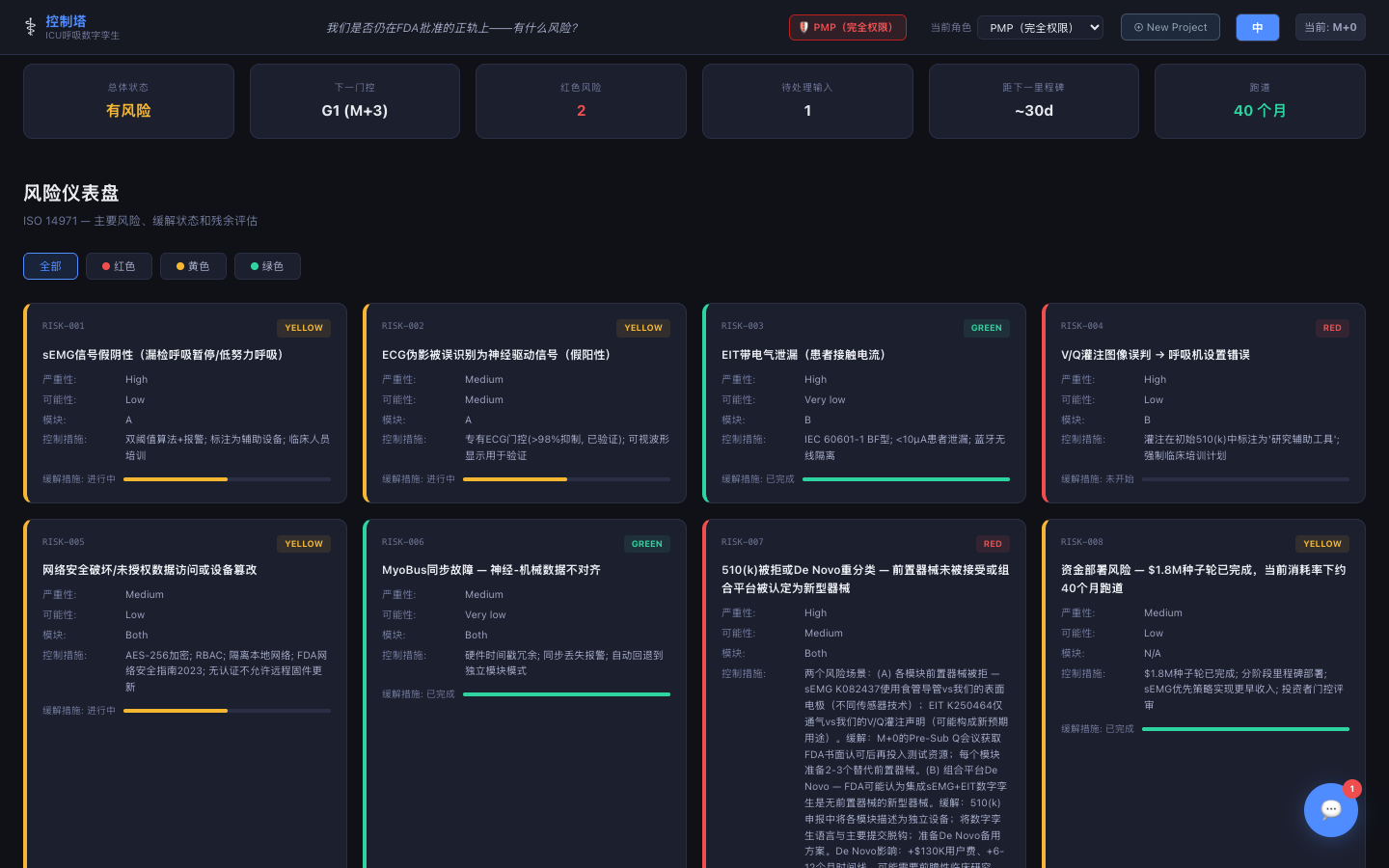
风险仪表盘
ISO 14971风险矩阵,含严重性、概率和颜色编码风险级别——从识别到关闭跟踪缓解措施。
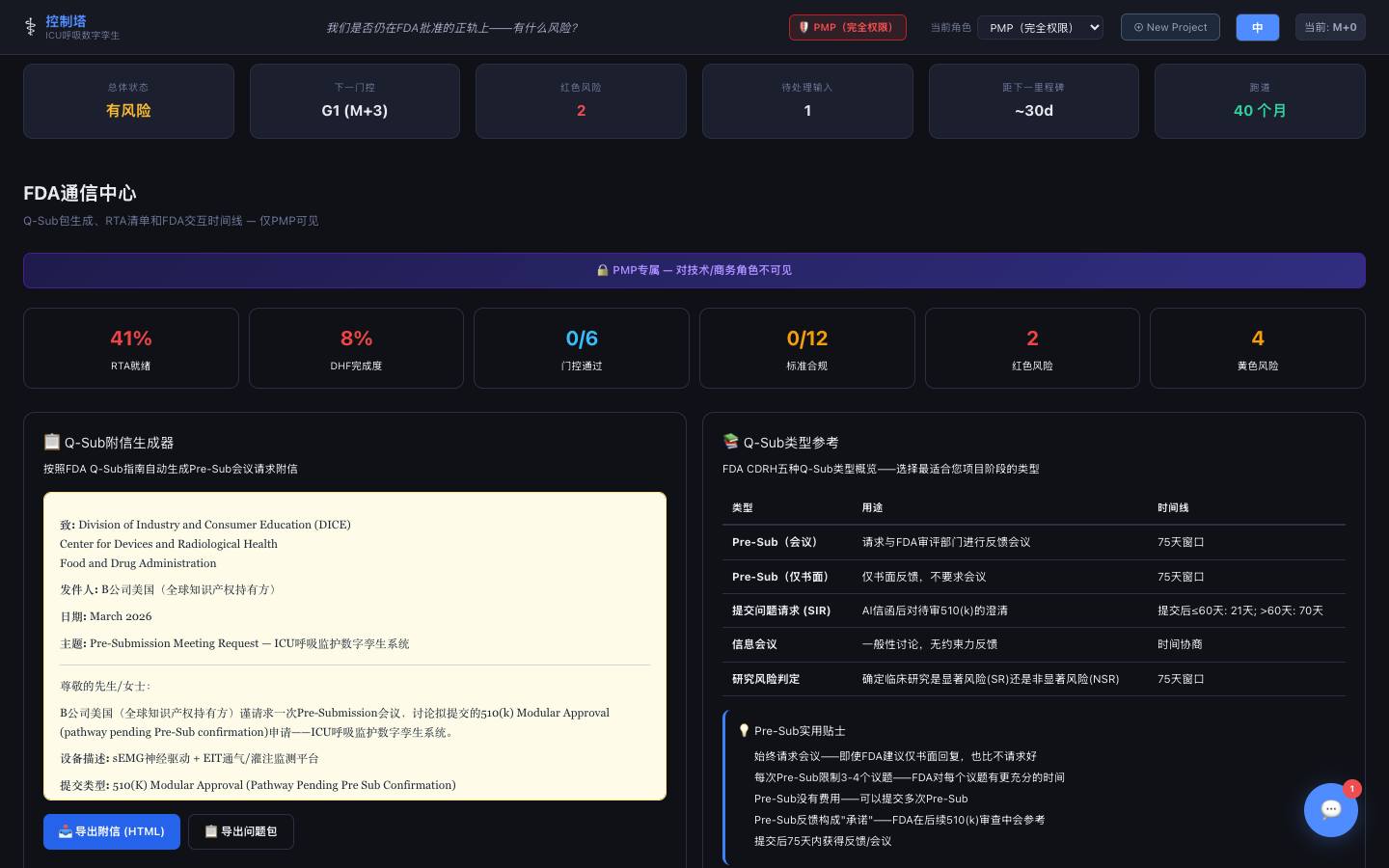
FDA通讯中心
Q-Sub附信生成器、17项RTA自检、MDUFA 90天径向时钟仪表(颜色编码: 第15天RTA筛查 → 第60天实质审查 → 第90天决定目标,含时钟暂停跟踪)、SE决策流程图,以及时间线标签页上的迷你日期徽章——集于一个平台。
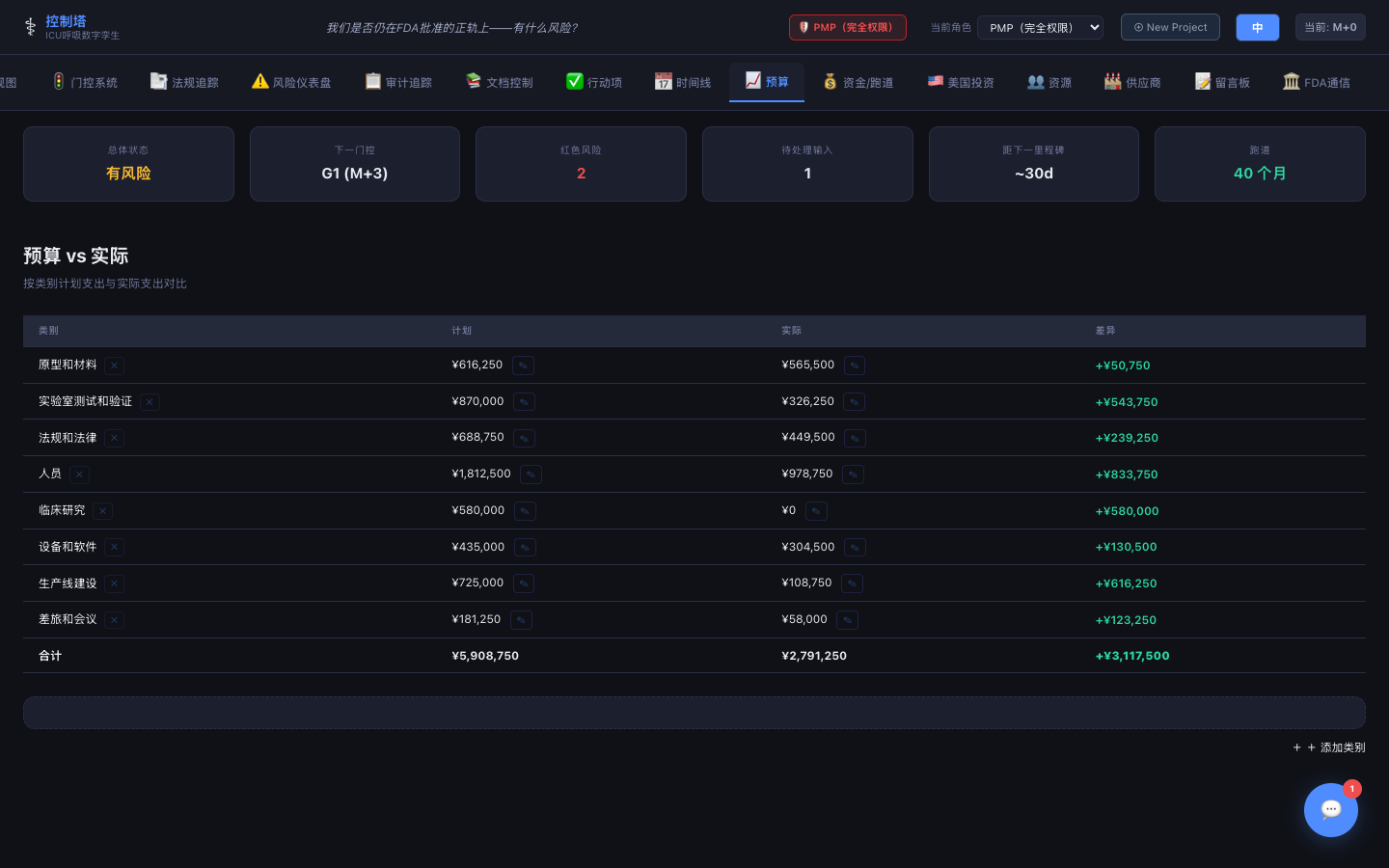
预算跟踪
按类别的计划与实际支出及自动差异计算——在USD和CNY显示之间切换。
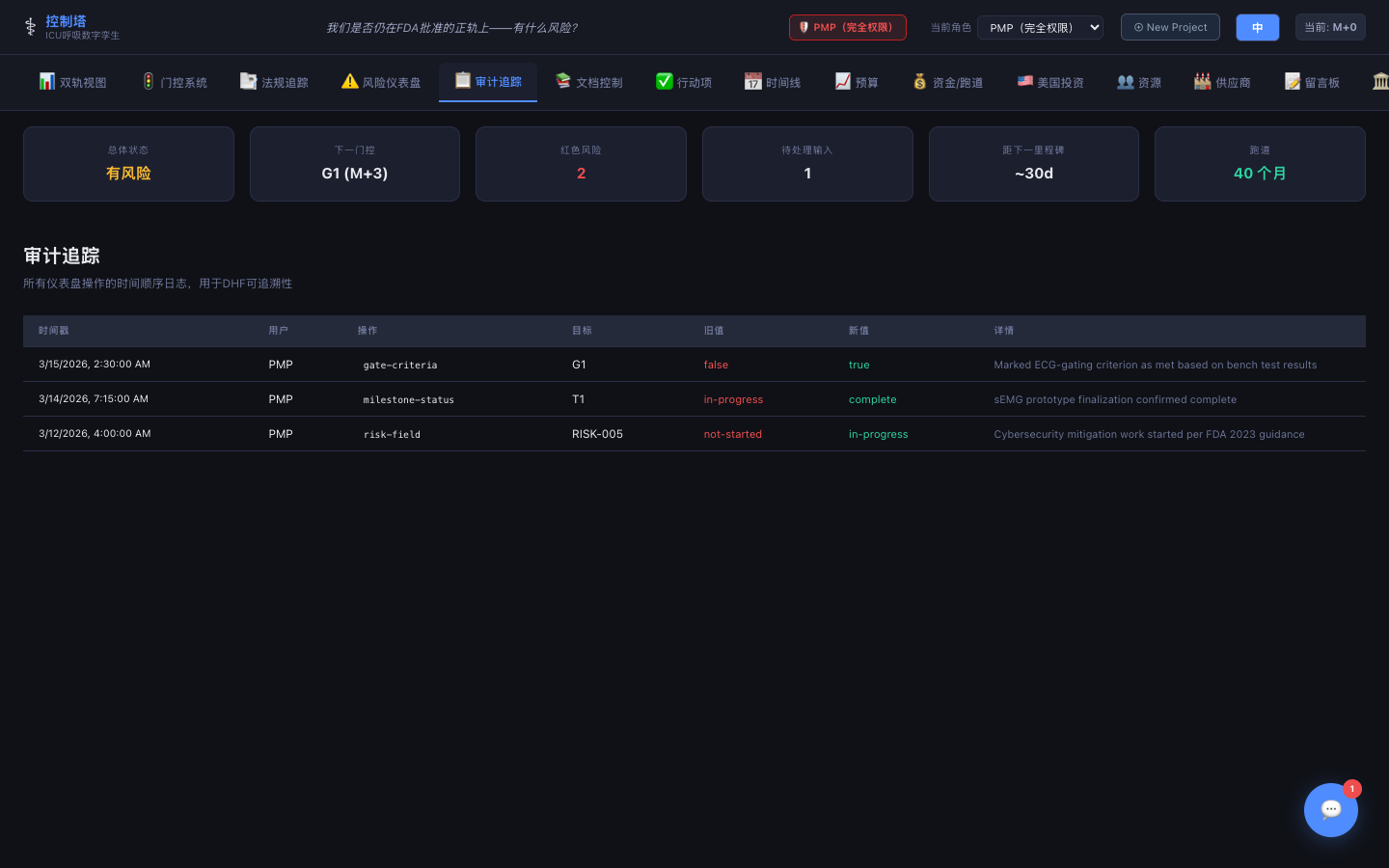
审计追踪
符合21 CFR Part 11——每次更改都有时间戳,记录用户、字段、旧值、新值和详细描述。
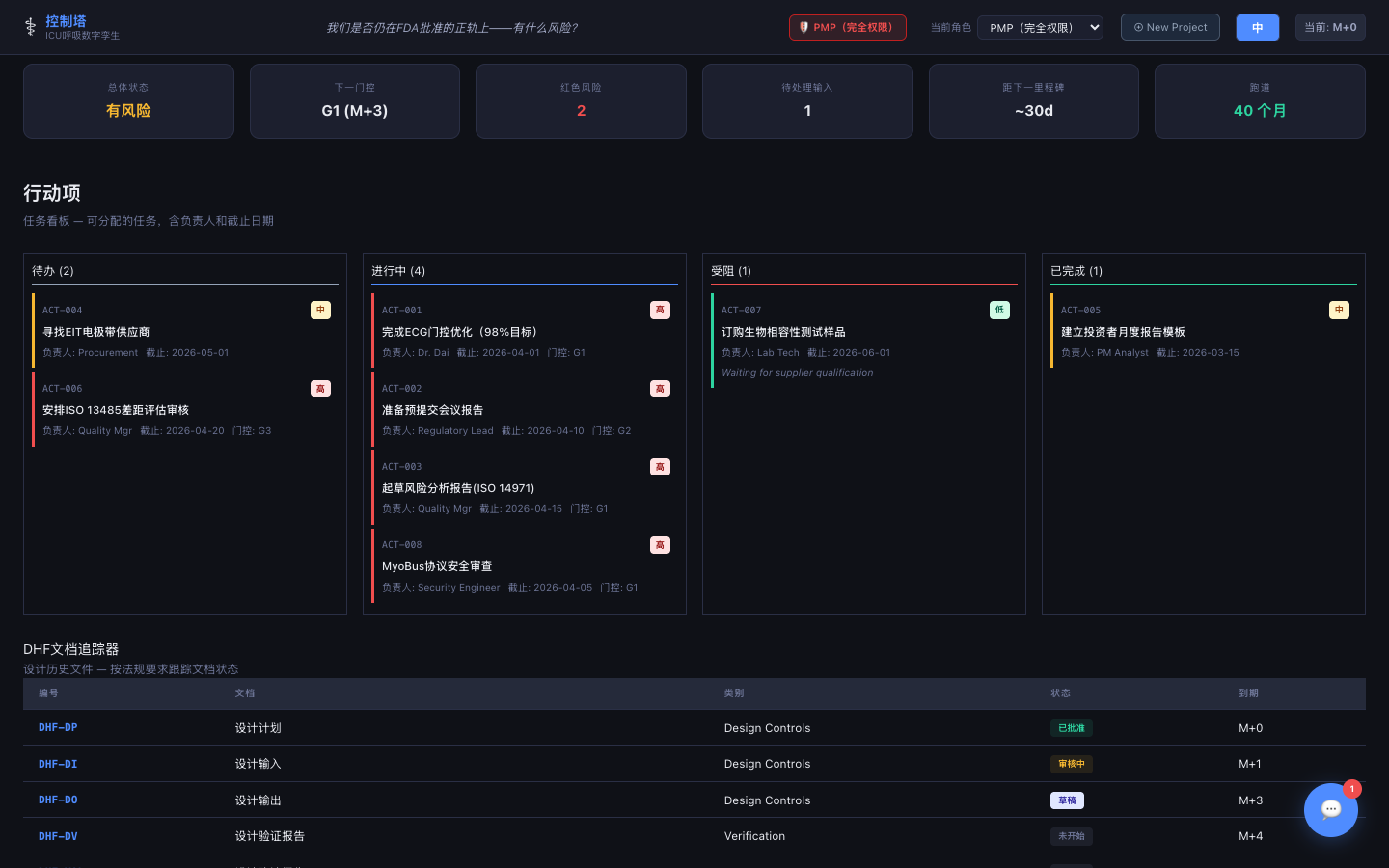
行动项 / DHF / CAPA
任务板、设计历史文件跟踪器、设备主记录跟踪器以及纠正与预防措施日志。
全部17个标签——完整项目可视化
 双轨道
双轨道
 关门系统
关门系统
 风险仪表盘
风险仪表盘
 审计跟踪
审计跟踪
 文档控制
文档控制
 行动项
行动项
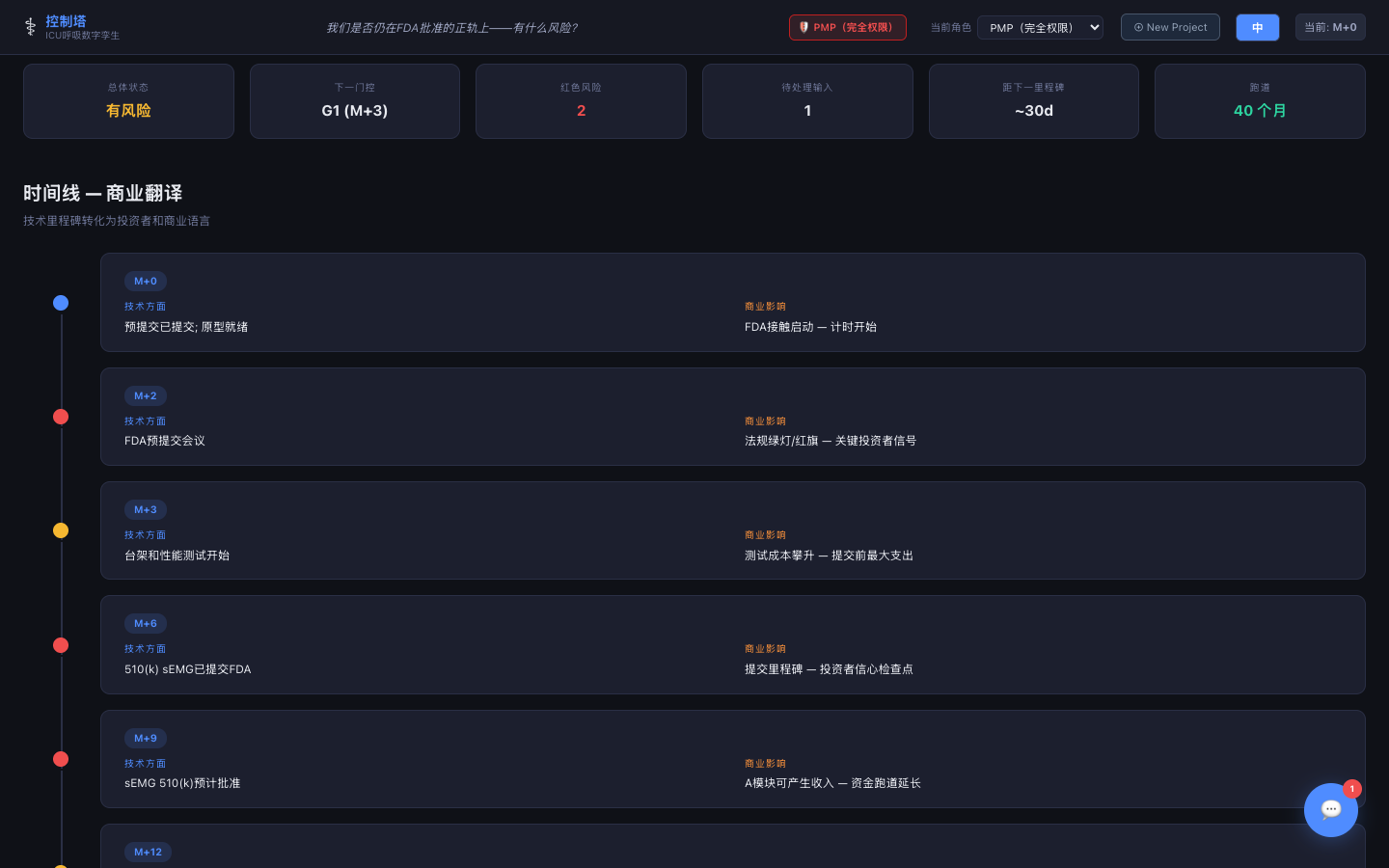 时间线
时间线
 预算
预算
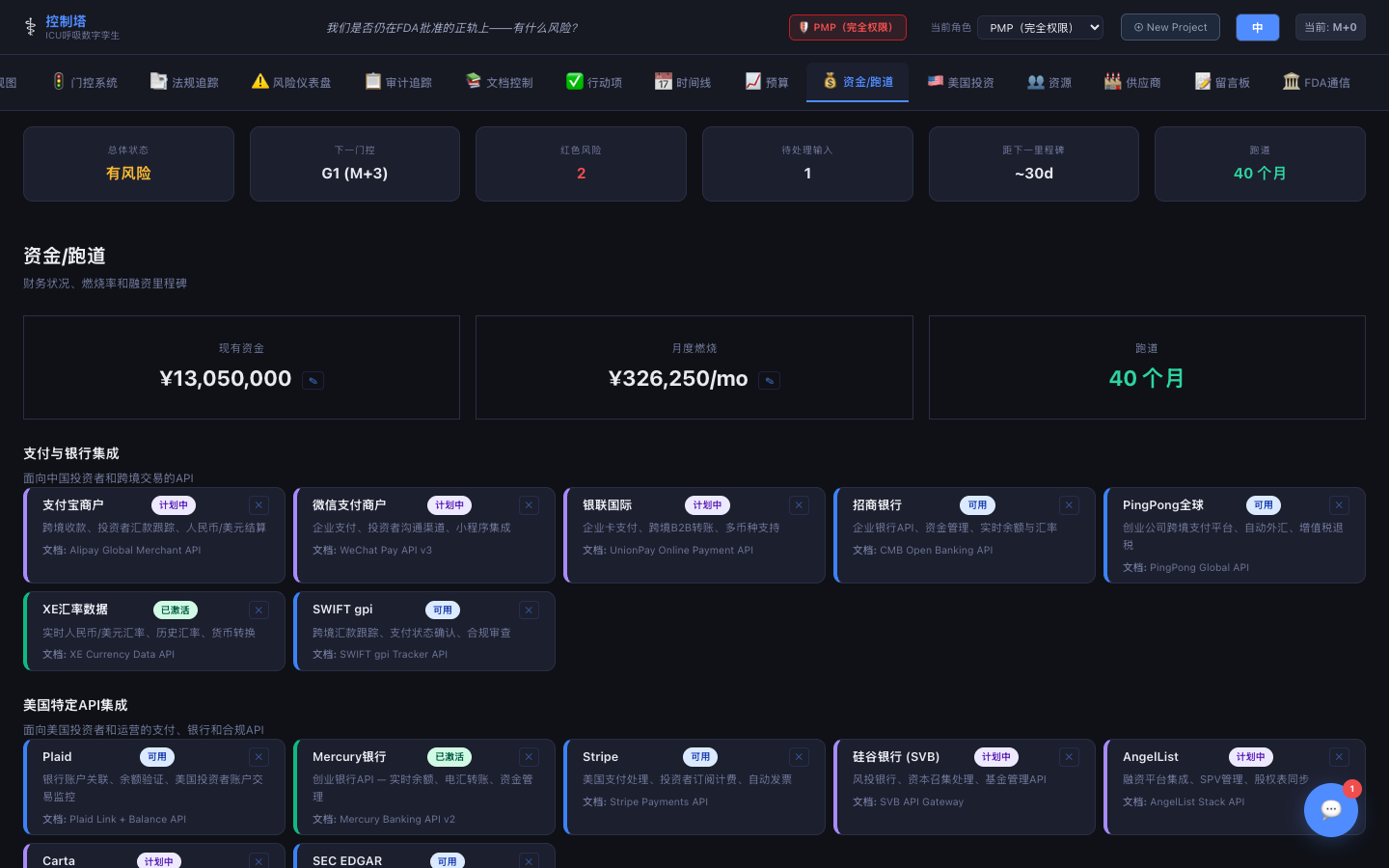 现金/跑道
现金/跑道
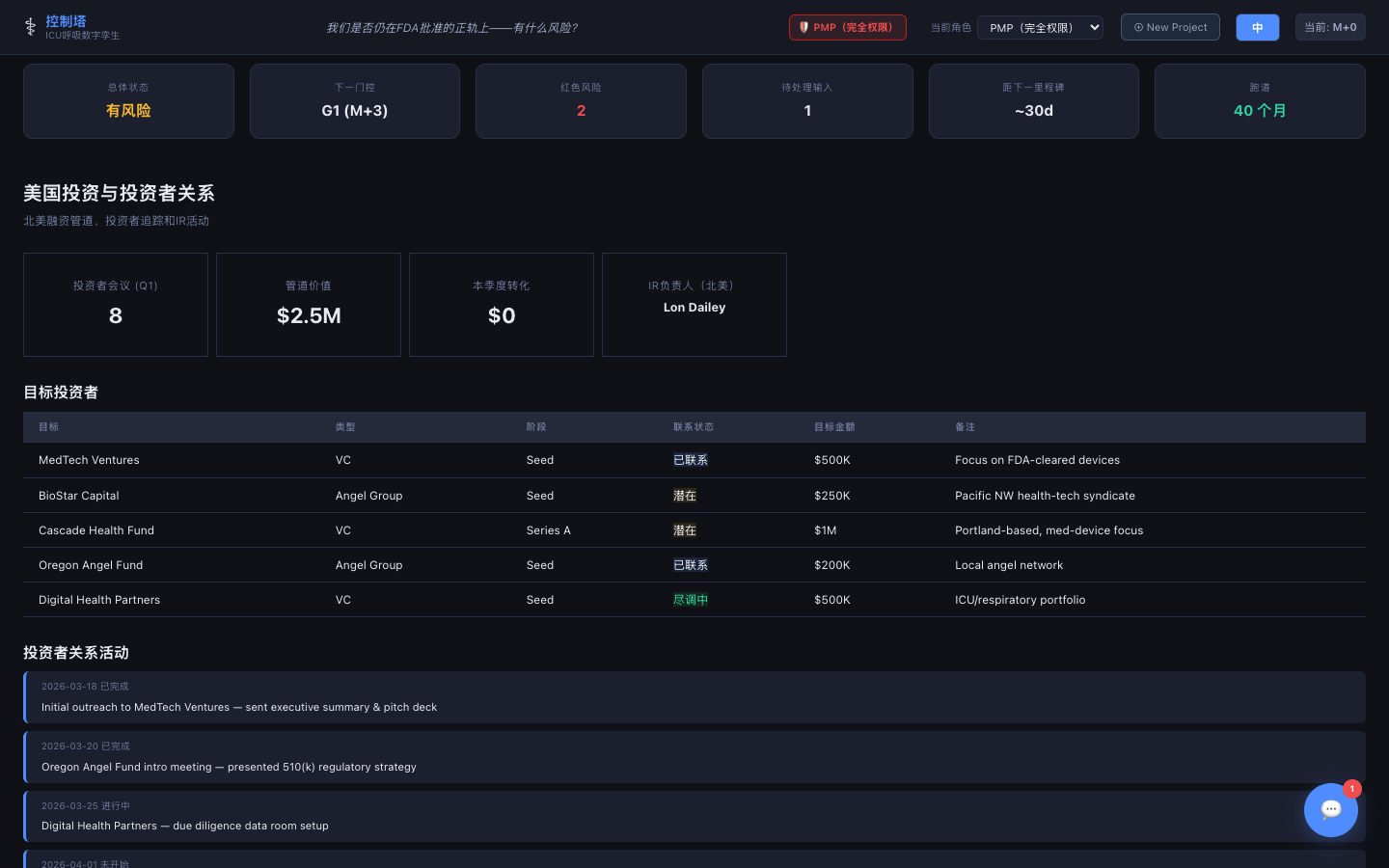 美国投资
美国投资
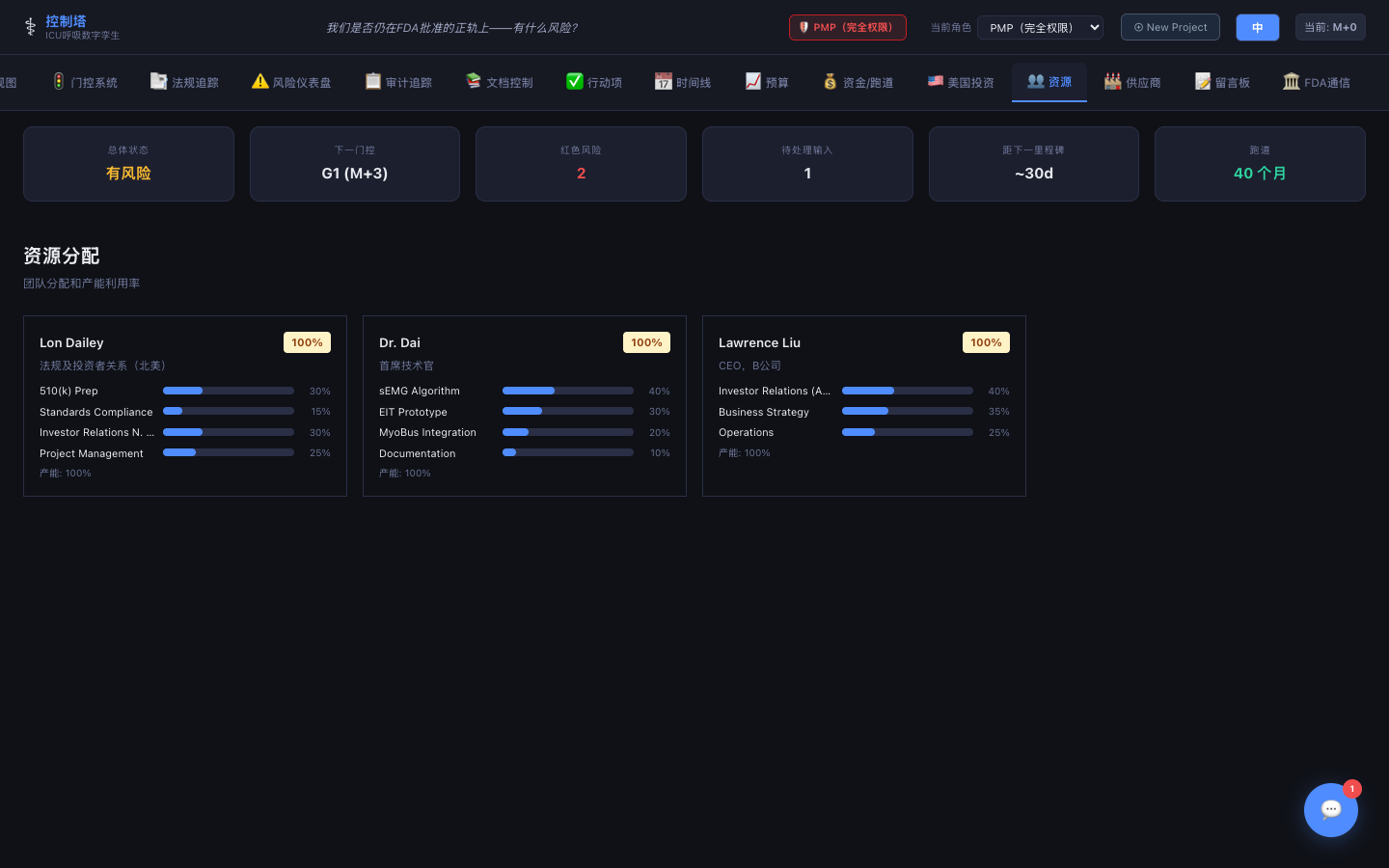 资源
资源
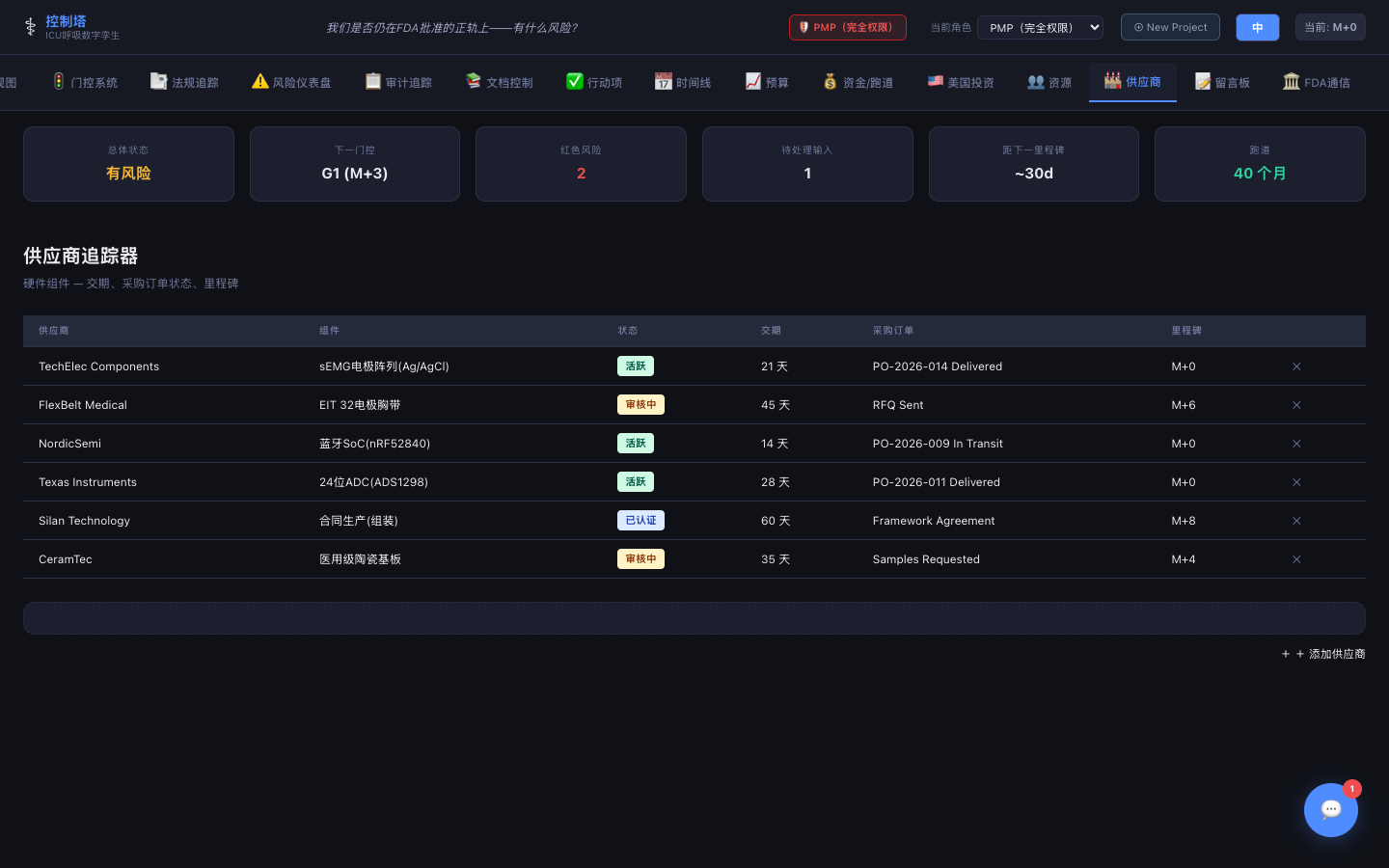 供应商
供应商
 消息中心
消息中心
 FDA通信
FDA通信
